連載
一覧生命を支える様々なメカニズム ~プログラム細胞死から神経難病まで~【第2回】

林田 直樹(はやしだ なおき) 山口大学 大学院 医学系研究科
ヒトの生を維持するプログラム細胞死(続編)
アポトーシス研究は精巣から始まった
前回(連載第一回)では、プログラム細胞死全体の、大まかな紹介をしました。今回はもう少し踏み込んで行きたいと思います。
前回の最後に、私の古い実験データ(2006年のもの)をお見せしました。「マウスの精巣で、アポトーシスが起きている」ことを示す組織の図です。茶色に染まっているのが、アポトーシスを起こした細胞です。
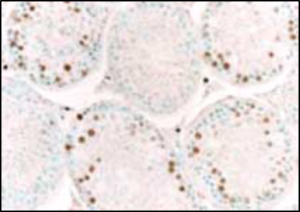 「精巣で細胞死が起こる」ことを不思議に思う方も多いでしょう。しかし精巣では、最終的に精子が出来るまで、75%の細胞がアポトーシスで死んでいくことが1978年には報告されています。アポトーシスが論文として発表されたのが1972年ですから、かなり早くから、「精巣において、ネクローシスとは明らかに違う細胞死がある」ことが、すでに研究されていたと考えるのが自然です。
「精巣で細胞死が起こる」ことを不思議に思う方も多いでしょう。しかし精巣では、最終的に精子が出来るまで、75%の細胞がアポトーシスで死んでいくことが1978年には報告されています。アポトーシスが論文として発表されたのが1972年ですから、かなり早くから、「精巣において、ネクローシスとは明らかに違う細胞死がある」ことが、すでに研究されていたと考えるのが自然です。
実は、1972年にアポトーシスを発見したイギリス人の Kerr らは、その15年後に発表した論文において、すでに精巣の生殖細胞におけるアポトーシスとネクローシスのかなり詳細な解析の結果を報告しているのです。この経緯を見ると、「アポトーシス研究(プログラム細胞死研究)は、精巣から始まった」と言っても良いでしょう。
アポトーシス研究は1990年代に爆発的に進みますが、アポトーシスを起こす細胞が他にもあることは、1990年代に入る前にすでに知られるようになっていました。文献をたどって行きますと、1974年には、すでにオタマジャクシ(英語では tadpole と言い、今でも実験では結構使われることが少なくないです)でのアポトーシスの論文が発表されています。続く1975年には、マウスのがん細胞に対して抗がん剤を投与したときに起こるアポトーシス、翌1976年には、ウイルス感染をさせたマウス同士で交配をさせると、胎児の組織(細胞)でアポトーシスが起き、胎児が育たない(妊娠が維持されない)ことまで報告されています。
この時期の論文は、実験系(どんな実験をどんなやり方、どんな順番で進めていくか)が今と比べて非常に単純なため、昨今のように「研究不正」などは起きにくい状況にありましたが、反面、研究者の数が今と比べてはるかに少なかったため、「実験データは正しくても、この実験で、こんな結論が導けるのか」という点には難があったと言えると思います。とはいえ、1970年代後半になると、毎年アポトーシスの論文が発表されるようになり、80年代までは、多くの細胞や組織でアポトーシスが起きるという、現象面のデータが蓄積され、90年代に入ると、ついに、「アポトーシスの起きるメカニズムの解明」に、進んでいったわけです。
アポトーシス(プログラム細胞死)が人を惹きつける?
少し本筋を外れて非科学的な話になりますが、最近、ネット上に公開されているアマチュア小説家の人の作品を眺めていますと、「アポトーシス」という言葉を使っている作品があったり、タイトル自体を「アポトーシス」としている方もいることに少々驚きました。なぜアポトーシスに惹かれ、アポトーシスをキーワードにした作品を書かれるのでしょうか?
これは私の想像になってしまうのですが、1つには、「アポトーシス=死」であることが重要なのだと思います。「死」をテーマとした作品は、これまで多く書かれてきましたが、「死」は、小説を含む文学的作品に置いて、「はかなさ」や「悲しさ」だけでなく、「美しさ」や「甘美な雰囲気」を与えています。さらにアポトーシスは「(細胞の)自殺」であり、かつ周囲に迷惑をかけない自殺の仕組みです。この性質を社会に投影し、「社会に何の足跡も残さず、ただ消えていく」と書き換え、そこに「美しさ」と「哀しさ」さらには、「最終的にはそうならざるを得ない、やるせなさと社会への怒り」の意味合いまで含めて、その意味合いに多少の違いはあるものの、おおよそ根幹的には同じ感傷的な意味合いを込めて「社会的アポトーシス」といった表現を使っている作品も複数見られました。
かなり話がずれてしまいますが、今の時代、「自分とは何か」「自分の存在意義とはなんだろうか、そのようなものはそもそもあったのだろうか?」という苦しみを持つ方が、各世代におられます。正直言えば、私自身「自分の存在意義」「自分が生まれてきた意味は何なのだろうか?意味があったとしても、その役割はもう終わってしまって、今はただ消化試合の人生を生きているだけではないのか?」と思うことがあります。自分は非常に死を恐れていますので、アポトーシスしたいとは思いませんが、上記のような人々がたくさんいて、彼らがそう考えることに対しては何の不思議もありません。この連載は「生命」をテーマにしていますので、こういった話に触れても良いのではないかと思い、私の思うところを書かせて頂きました。正直言えば、私もかつては、小説家を目指した少年の1人であり、アマチュアの小説家の方たちが、アポトーシスに興味を持つ、あるいは医学・生物学的な意味合い以上のものをアポトーシスに見出すことは結構自然なことなのではないか、と個人的に感じたのです。
プログラム細胞死の中でも、アポトーシスを起こす経路は他にもある
ここでは本筋の方に戻りまして、私の「プログラム細胞死研究」についても紹介したいと思います。一部はすでに論文として発表していますが、今現在研究途中で、「この細胞の死に方は、これまで知られているプログラム細胞死に当てはまるのか、それともネクローシスなのか?」と迷っているデータについても、ほんの少しその悩みをお話ししたいと思います。
私がアポトーシスそのものを扱った論文を発表したのは、2006年のことになります(今回も冒頭で紹介した、精巣のアポトーシスの実験を行った論文です)。一ヶ月に300から400時間という、あとで計算して自分でも驚いたほどの実験時間(労働時間)をかけることによって、この論文は完成しましたが、この時に実験によって発見したアポトーシスの起こり方が、すでに広く知られていたメカニズムとは部分的には一致するものの、それ以外の面では明らかに異なっていたのです。
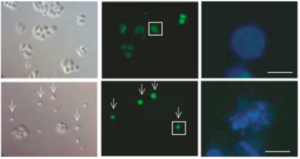 左の図は、その論文のデータの中の1つです。アポトーシスを起こす遺伝子として、Tdag51(T-cell death associated gene 51の。遺伝子名などは、最初の発見者が自由に決めてよいものなので、遺伝子名は、「ああ、そういう名前なんですね」くらいの理解で十分です)というものが7年前に発表されていました。しかし、その著者らが続いて「細胞を培養して実験すると、アポトーシスは観察される。しかし、マウスでこの遺伝子を無くさせても、特に問題は無いようだ」という論文を出していたので、私は Tdag51 が本当にアポトーシスを起こすのかどうかを確かめるところから実験を始めました。それがこの図です。Tdag51 は、それがつくられていることをわかりやすくするために、GFP(緑色蛍光タンパク質。日本人の下村博士によって発見され、この功績により、博士はノーベル賞を授与されました)をつなげて緑色に光るようにして、細胞に発現させ(作らせ)ました。
左の図は、その論文のデータの中の1つです。アポトーシスを起こす遺伝子として、Tdag51(T-cell death associated gene 51の。遺伝子名などは、最初の発見者が自由に決めてよいものなので、遺伝子名は、「ああ、そういう名前なんですね」くらいの理解で十分です)というものが7年前に発表されていました。しかし、その著者らが続いて「細胞を培養して実験すると、アポトーシスは観察される。しかし、マウスでこの遺伝子を無くさせても、特に問題は無いようだ」という論文を出していたので、私は Tdag51 が本当にアポトーシスを起こすのかどうかを確かめるところから実験を始めました。それがこの図です。Tdag51 は、それがつくられていることをわかりやすくするために、GFP(緑色蛍光タンパク質。日本人の下村博士によって発見され、この功績により、博士はノーベル賞を授与されました)をつなげて緑色に光るようにして、細胞に発現させ(作らせ)ました。
上の3つの細胞の図は、GFP のみが細胞内で出来ている場合のものです。一番左は普通の顕微鏡で見た映像、真ん中は蛍光顕微鏡というものを使って、GFP にある特定の波長の光を当てて光らせることにより、GFP が出来ている細胞が明瞭に見えるようになっています。一番右は、核の中のクロマチンという、DNA のかたまりが青色に見えていると思って下さい。GFP は特に細胞を殺すような毒性は見つかっていないタンパク質ですので、これを作っている細胞はシャーレにきちんと張り付いていますし(この実験ではシャーレの底に張り付くタイプの細胞を用いました)、それは蛍光顕微鏡でも変わらず、また、クロマチンも均等に青色に染まっており、正常の状態です。
ところが、Tdag51 に GFP をつなげて、細胞内に作らせたのが下の3つの図なのですが、左と真ん中の図において矢印で示されているように、丸い細胞が存在しています。この丸い細胞は死んでいる細胞です。さらに、一番右の図を見ますと、青色で染まった核の中に、不均一な塊が見えます。これは実はクロマチンであり、このような異常な形のクロマチンが観察されるのもアポトーシスの特徴です。この結果によって、「自分の実験でも Tdag51 がアポトーシスを起こすことが示された。Tdag51 は、アポトーシスを細胞に起こす遺伝子だ」と、自信を持って次の実験に進んだわけです。
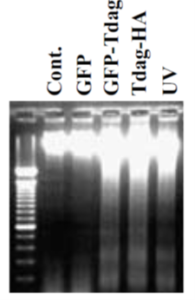 次の実験データは、左の黒い背景のデータです。これが「DNA の電気泳動」という実験で、いわゆる「分子生物学」と言われる分野の実験方法としては基本的なものです。この簡便さが、分子生物学が爆発的に世界中に広まった大きな理由の1つです(手前味噌ではありますが、左の電気泳動図を実験で再現するのは結構難しいです)。ここでは、一番左から3番目の「GFP」と書いてあるところの下の部分と、その右の「Tdag」の文字が含まれている2つの場所の下の部分を比べて下さい。GFP の下の部分はほぼ真っ黒で、これは、ここには DNA がほとんどないことを示しています。
次の実験データは、左の黒い背景のデータです。これが「DNA の電気泳動」という実験で、いわゆる「分子生物学」と言われる分野の実験方法としては基本的なものです。この簡便さが、分子生物学が爆発的に世界中に広まった大きな理由の1つです(手前味噌ではありますが、左の電気泳動図を実験で再現するのは結構難しいです)。ここでは、一番左から3番目の「GFP」と書いてあるところの下の部分と、その右の「Tdag」の文字が含まれている2つの場所の下の部分を比べて下さい。GFP の下の部分はほぼ真っ黒で、これは、ここには DNA がほとんどないことを示しています。
一方、「Tdag」の文字が含まれた、「GFP-Tdag」と「Tdag-HA」文字の下を見て下さい。やや薄く、太さも少々ことなりますが、白い色で、はしごのように横線が入っているのが見えるでしょうか。この横線が「DNA」であるのですが、正常な細胞では、DNA がこのように見えることはないのです。「GFP」の文字の下の部分(これを「レーン」と呼びます。スポーツのボーリングの「レーン」と同じです)にはほとんど光るもの (DNA) が見られない。これが正常なのです。
Tdag の文字が含まれたレーンで、はしごのような横線がいくつか見えるこのような像を「DNA ラダー(ラダーは「はしご」の意味)」と呼び、これが実験で観察されることがアポトーシスの現象の大きな特徴でもあります。このようにきれいに DNA ラダーが見えるのは、細胞内にある酵素タンパク質が、自分の細胞の DNA をある程度の大きさごとにいくつも切ってバラバラにしているからなのです。DNA がバラバラに切れたら細胞はもちろん生きていけません。まさに細胞の自殺です。これは、日本人の長田重一先生の研究グループによってメカニズムも解明されており、アポトーシスの中でも最も特徴的と言えるのではないでしょうか。
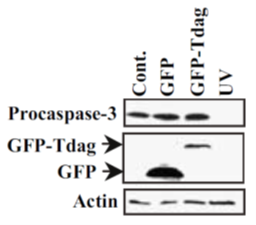 問題は左のデータでした。これは「ウェスタンブロット」と言いまして、タンパク質を検出・解析する方法としては最も基本的なものの1つです。黒く太い横棒(これを「バンド」と言います)があれば、それは「そのタンパク質(ここでは横に英語で書かれた名前のタンパク質)が存在する」ことを示します。この実験によっても、アポトーシスの特徴を再現しようとして実験しました。
問題は左のデータでした。これは「ウェスタンブロット」と言いまして、タンパク質を検出・解析する方法としては最も基本的なものの1つです。黒く太い横棒(これを「バンド」と言います)があれば、それは「そのタンパク質(ここでは横に英語で書かれた名前のタンパク質)が存在する」ことを示します。この実験によっても、アポトーシスの特徴を再現しようとして実験しました。
ところが、データが示した結果は、典型的なアポトーシスとは違うものでした。アポトーシスが起きる場合、DNA がバラバラに切られる以外に、「カスパーゼ」という、アポトーシスを起こすのに重要な別のタンパク質が働きます。このカスパーゼにはいくつか種類があるのですが、中でも「カスパーゼ3」がアポトーシスには重要なものであることがわかっています。しかしアポトーシスが起きない状態では、データにあるように「procaspase-3(カスパーゼ3前駆体)」の状態にあります。この状態ではカスパーゼ3は働きませんが、アポトーシスを起こす段階になると、カスパーゼ3前駆体は切断されてなくなり、実際に働くカスパーゼ3が登場します。「切断されてなくなる」と言うことは、このウェスタンブロットの図で言いますと、「GFP-Tdag」の文字のすぐ下のレーンから、「カスパーゼ3前駆体のバンドが消えてなくなる」はずです。ところがこのデータでは、カスパーゼ3前駆体のバンドがはっきり見えている、言い換えれば「カスパーゼ3前駆体は、アポトーシスが起きても存在し続けている」ことを示しているのです。
アポトーシスの起こるメカニズムは複数あるという認識がすでにこの頃にはあったので、特に焦ることはありませんでしたが、とはいえ、「Tdag51 が起こすアポトーシスは、典型的なアポトーシスではない」ことを示す重要なデータですから、繰り返し同じ実験を行い、その全ての結果が一致したため、自信を持ってこのデータを論文に入れました。
現在私は、神経変性疾患(神経難病)のアルツハイマー病やハンチントン病、前頭側頭型変性症 (FTLD) を中心とした、認知症状が起こり、神経細胞の細胞死が起こる病気の起こるメカニズムと、これらを完治させるための治療薬・治療方法の開発を目標として研究を行っていますが、これらの病気で起きている神経細胞の細胞死が、アポトーシスなのかそれとも別のプログラム細胞死なのかがまだわからないのです。まだ研究途中ですので多くは申し上げられませんが、Tdag51 の解析も含めて行っているものの、思った以上に難しいと感じています。治療薬の開発が最も重要な目的ではありますが、病気の起こるメカニズムを詳細に明らかにすることは、副作用が少ない一方で効果は大きい薬剤の開発につながりますので、この連載を続けている間も、一生懸命研究を行いたいと思います。
